48. Consider the reaction 3A + B + C → D + E where the rate law is defined as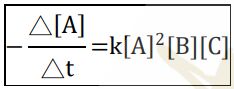
An experiment is carried out where [B]0 = [C]0 = 1.00 M and [A]0 = 1.00 × 10–4 M. After 3.00 minutes, [A] = 3.26 × 10–5 M and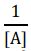 = 3.067 × 104 . The value of k is :
= 3.067 × 104 . The value of k is :
(A)6.23 × 10–3 L3 /mol3 ·s
(B) 3.26 × 10–5 L3 /mol3 ·s
(C) 1.15 × 102 L3 /mol3 ·s
(D)1.00 × 108 L3 /mol3 ·s
(E) None of these
答案:登入後查看
統計: A(0), B(0), C(1), D(1), E(0) #3840058
統計: A(0), B(0), C(1), D(1), E(0) #3840058
詳解 (共 3 筆)
#7318282
請參考義守後中類似題
當其中一個濃度遠遠遠大於另一個,可以把高濃度的視為定值(常數)下去做計算
ㅤㅤ
11. 已知反應 A + B → C + D 的速率定律式 rate = k [A][B],k = 100 M-1 s -1。假設進行該反應時,起始濃 度[A]o = 0.001 M,[B]o = 0.1 M,則 _____。 (ln 2 = 0.693)
(A) 100 s 時,[A] = 10-4 M
(B) 偽一級(pseudo-first order)反應速率常數 kobs = 0.1 s-1
(C) 此反應的半生期(half life)為 0.0693 s
(D) 若將[A]o 提升為 0.005 M,反應的偽一級速率常數 kobs = 50 s-1
-107年 - 義守大學 107 學年度 學士後中醫學系 入學招生考試試題-化學#69825ㅤㅤ
答案:C
ㅤㅤ
0
0